Avances
EFECTOS SECUNDARIOS
COVID-19: EMA reitera su apoyo hacia el uso de la vacuna de Janssen
El organismo asegura que los beneficios del biológico superan los riesgos de los efectos secundarios, los cuales han sido poco frecuentes
Martes, 20 de abril de 2021, a las 17:15
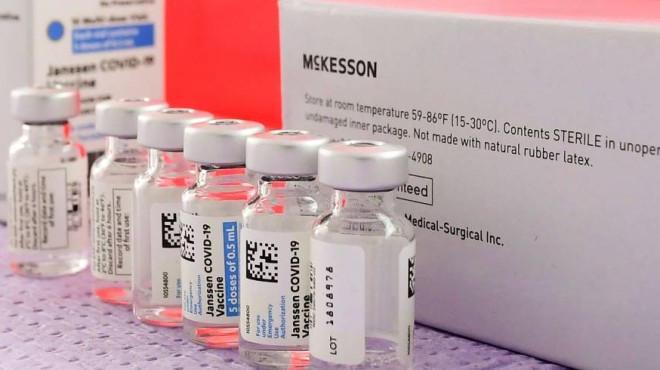
La EMA afirma que hay mayores beneficios en el uso de la vacuna de Janssen. |
Redacción. Bogotá
La Agencia Europea del Medicamento (EMA por sus siglas en inglés) se ha manifestado con respecto a los casos de trombos reportados, tras la aplicación de la vacuna contra la COVID-19 de Janssen filial de la empresa Johnson & Jonhson.
La EMA encontró un “posible vínculo” con los coágulos sanguíneos reportados en Estados Unidos, pero confirmó que sus beneficios siguen mayores.
Por ello, la Unión Europea (UE) recibirá nuevamente la vacuna que no había sido aplicada en otros ciudadanos mientras se esperaba el aviso de la EMA, incluyendo información sobre sus contraindicaciones.
Cabe destacar que, el concepto de la agencia no ha limitado su uso a ningún grupo de edad más allá de los 18 años, sin embargo, el Gobierno de cada país será el responsable de decidir si aplica o no el biológico en su territorio.
El organismo también ha señalado que, se basó en el estudio de ocho casos que se reportaron en Estados Unidos sobre las más de siete millones de vacunas aplicadas, concluyendo que la aparición de coágulos sanguíneos es un efecto secundario muy raro.
Sin embargo, la EMA ha afirmado que los episodios poco frecuentes de coágulos y bajos niveles de plaquetas deben indicarse en el prospecto del producto. De igual forma, el organismo confirmó que todos los casos de trombos se presentaron en personas de 60 años, la mayoría de ellas mujeres.
“Según la evidencia actualmente disponible, no se han confirmado factores de riesgo específicos”, ha destacado el comunicado de la EMA.
La vacuna de Jonhson & Jonhson debió empezar a distribuirse en la UE desde la semana pasada, pero se detuvo, ya que, la compañía suspendió el reparto hasta que se aclararan los casos de trombos como efecto adverso. El pasado 13 de abril la FDA y los Centros de Control y Prevención de Enfermedades (CDCP) suspendieron el uso del biológico para investigar los casos.
En ese sentido, la EMA adelantó y emprendió el estudio antes de que el medicamento se empezara a administrar en Europa, pese a que la vacuna ya está autorizada en algunos países de la UE como Bruselas.
Sobre los coágulos sanguíneos
Por su parte, los Expertos de la EMA han explicado que los coágulos se produjeron en zonas anatómicas inusuales, como en las venas del cerebro (trombosis del seno venoso cerebral) y el abdomen (trombosis de la vena esplácnica) y en las arterias, junto con niveles bajos de plaquetas en sangre y, a veces, se produjo sangrado.
“Los casos revisados fueron muy similares a los que ocurrieron con la vacuna del COVID-19 desarrollada por AstraZeneca, Vaxzevria”, ha señalado el comunicado del organismo.
Asimismo, la EMA ha estipulado que, los coágulos sanguíneos y plaquetas bajas se observan a veces en pacientes con heparina llamada trombocitopenia inducida por heparina, de cualquier modo, el uso de cualquier medicamento en la UE está respaldado por una evaluación científica realizada por el organismo para asegurarse que su uso es seguro y eficaz.
La EMA ha relacionado los casos de trombos con la aplicación de la vacuna de Janssen, pero respaldó su uso, ya que, sus beneficios son mayores que los riesgos, además de presentarse con muy poca frecuencia, mientras tanto, la gigante estadounidense busca producir 1.000 millones de dosis en 2021.La UE acordó la compra de 200 millones de dosis, más otros 200 millones adicionales.