Gestión
FASE 2
Más de 100 respiradores mecánicos creados en Medellín listos para ser usados en pacientes con CoVID19
Luego de 10 meses de investigación científica y ensayos clínicos, el Invima decidirá si pueden ser o no comercializados.
Lunes, 28 de diciembre de 2020, a las 16:36

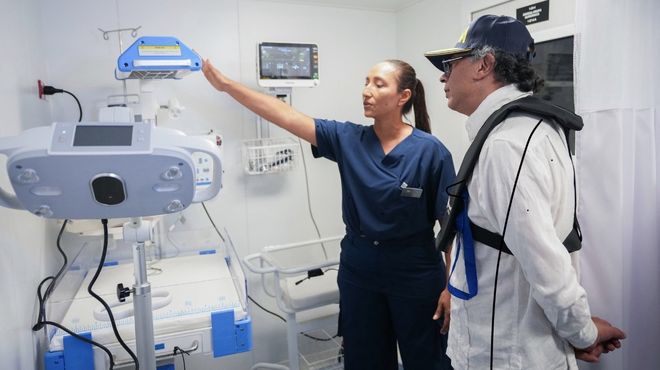
Luis Horacio Atehortúa, principal investigador del proyecto. |
Redacción. Bogotá
De acuerdo con la Universidad de Antioquia, los ventiladores mecánicos han sido calificados como dispositivos terapéuticos fundamentales para hacerle frente a la pandemia por CoVID19, especialmente para la atención de pacientes que presentan una condición grave, como ha sido el caso de algunos pacientes con complicaciones respiratorias agudas.
Según ha señalado el Grupo de Investigación en Bioinstrumentación e Ingeniería Clínica de la Universidad de Antioquia (GIBIC), esto ha dado pistas del impacto social que tiene la donación de 106 ventiladores mecánicos ‘GIBIC Neuma V1.0’, a clínicas y hospitales principalmente de Medellín, luego del trabajo maratónico llevado a cabo por el GIBIC.
El punto de partida, tras los primeros casos de CoVID19 en el país, conforme ha destacado la Universidad de Antioquia, ha sido integrar la alianza ‘InnspiraMED’ coordinada por ‘Ruta N’ y conformada por la universidad, Industrias Médicas Sampedro y la Universidad EIA, con el objetivo de procurar que ningún colombiano muriera por la falta de un ventilador mecánico en una Unidad de Cuidados Intensivos (UCI).
Es así que, luego de 10 meses de investigación científica y ensayos clínicos, los ventiladores mecánicos creados en Medellín están listos para ser aprobados por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima). La entidad tendrá que decidir si los respiradores pueden ser comercializados o no, una vez que hayan sido probados en pacientes con CoVID19 y que hayan sido internados en las UCI.
Esta sería la segunda fase de prueba, ya que, la primera consistió en someter a un ensayo a cada uno de los 3 prototipos de InspiraMed. Para cumplir con las exigencias del protocolo aprobado por la autoridad sanitaria para la Fase 1, fueron reclutados 5 pacientes para el prototipo de la Universidad de Antioquia, 5 para el de la Universidad EIA y la misma cantidad para el de Industrias Médicas Sampedro. Estas pruebas se desarrollaron en el Hospital San Vicente Fundación, la Clínica Bolivariana y la Clínica las Américas.
Lea: Ventiladores mecánicos a bajo costo de la Universidad de Antioquia superan la prueba en animales.
Según ha manifestado el investigador principal del proyecto a medios locales, Luis Horacio Atehortúa, “los 3 modelos dieron excelentes resultados y no presentaron eventos adversos”, lo que quiere decir que ningún dispositivo ha presentado fallas o inconvenientes a la hora de ser usados en pacientes reales. Tras esas primeras pruebas que se desarrollaron con éxito, el equipo investigativo ha señalado que aun se necesitará organizar un informe técnico con los resultados del estudio para ser enviado al Invima.
“Es un paso muy importante para la investigación y desarrollo del ecosistema de ciencia, tecnología e innovación de Medellín. Esperamos tener consolidado el informe sobre los 15 pacientes en los que se ensayaron los 3 ventiladores en dos semanas máximo. Luego entrará a revisión por parte del Invima, el cual verificará si se puede dar apertura a la Fase 2 de Ensayos Clínicos”, ha indicado director ejecutivo de Ruta N, Javier Darío Fernández.
El equipo investigativo ha estipulado que, en caso de ser aprobados, los ventiladores se comercializarían entre 15 millones de pesos y 20 millones de pesos, lo que representaría un ahorro económico para el país si se compara con ventiladores con las mismas características que son importados en unos 50 millones de pesos.
Por su parte, el equipo de investigadores de InspiraMed ha denotado que para la fase 2 presentará un protocolo que incluya menos pacientes y menos tiempo conectados a los ventiladores pues “ya probamos que eran seguros y para eso sí se necesitaba una buena muestra y con buen tiempo, pero para probar que funcionan no necesitaríamos esas mismas características”, ha afirmado Atehortúa.
Dispositivos listos para ser usados en centros hospitalarios
No obstante, como los ventiladores desarrollados por la Universidad de Antioquia y la Universidad EIA (producidos por las empresas Auteco y Haceb, respectivamente) ya han cumplido con todos los requisitos de la fase 1, podrán ser usados en los centros hospitalarios.
“Siempre y cuando se agoten las posibilidades con las máquinas comerciales y exista un consentimiento del paciente o sus familiares”, según ha destacado la Circular Externa 031 de 2020, emitida por el Ministerio de Salud. Estas dos condiciones se mantendrán hasta que el Invima dé el permiso para la operación comercial de los 3 dispositivos, ya que, fue un proyecto presentado en conjunto por la alianza InnspiraMED. Así lo ha advertido Alher Mauricio Hernández, líder del Gibic.
Hernández también ha reiterado que cuando se completen las pruebas clínicas por parte de Industrias Médicas Sampedro y se reciba el visto bueno para adelantar la fase 2 del proyecto, “en un contexto como el actual, los tres prototipos entrarán a competir con los ventiladores comerciales”.
El dato
Según han enfatizado medios locales, el equipo dirigido por Atehortúa ha recalcado que tienen preocupación por una posible suficiencia en recursos para culminar la fase 2 que se avecina. Atehortúa ha asegurado que, los grandes patrocinadores que se habían unido a la causa, como Postobón, decidieron retirarse cuando el Gobierno Nacional empezó a anunciar la importación masiva de estos artefactos.